В работе на опыте исследуются статистические закономерности, которые наблюдаются в целом ряде явлений, в том числе во многих явлениях микромира. В области молекулярных явлений, например, им подчиняется распределение молекул идеального газа по скоростям и энергиям, если газ находится в равновесном состоянии.
Для этого типа закономерностей характерны два момента: во-первых, наличие большого, но конечного числа однородных объектов; во-вторых, то, что значение скорости молекулы газа не может быть определено однозначно: оно зависит от большого числа необходимых и случайных факторов. Однако, хотя значение скорости отдельной молекулы случайная величина, для большого числа молекул существует определенный закон их распределения по скоростям: скоростью в каждом возможном интервале значений обладает совершенно определенное число молекул при данной температуре.
В статистической теории существует понятие функции распределения,
с помощью которой можно рассчитать число молекул ![]() из общего
числа их
из общего
числа их ![]() , имеющих относительную скорость в некотором
бесконечно малом интервале скоростей
, имеющих относительную скорость в некотором
бесконечно малом интервале скоростей ![]() :
:
Функция распределения молекул газа по скоростям была найдена
английским физиком Д.Максвеллом и носит его имя. Для
относительных значений скорости она не зависит от рода газа и его
температуры и имеет вид:
Распределение Максвелла для абсолютных значений скорости имеет следующий вид:
Наиболее общие количественные стороны
статистических закономерностей изучаются теорией вероятностей.
Функция распределения называется плотностью вероятностей, а
отношение ![]() -- вероятностью данного случайного события.
-- вероятностью данного случайного события.
Таким образом, ![]() является, с одной стороны,
относительным числом молекул, имеющих значения относительной
скорости в бесконечно малом интервале значений
является, с одной стороны,
относительным числом молекул, имеющих значения относительной
скорости в бесконечно малом интервале значений ![]() , а с другой
стороны, вероятностью того, что некоторая молекула имеет значение
относительной скорости в интервале
, а с другой
стороны, вероятностью того, что некоторая молекула имеет значение
относительной скорости в интервале ![]() . Это отношение можно
рассчитать по известной функции распределения.
. Это отношение можно
рассчитать по известной функции распределения.
На рис.4.1 представлен график распределения Максвелла
для относительных значений скорости (52). На одной оси
отложены возможные значения скорости ![]() , а на другой --
соответствующие им значения
, а на другой --
соответствующие им значения ![]() . Максимум функции
соответствует наиболее вероятной скорости молекул, при этом
. Максимум функции
соответствует наиболее вероятной скорости молекул, при этом ![]() .
Число молекул с нулевой скоростью равно нулю; наибольшее число
молекул имеет скорости, близкие к наиболее вероятной. График
несимметричен относительно максимума.
.
Число молекул с нулевой скоростью равно нулю; наибольшее число
молекул имеет скорости, близкие к наиболее вероятной. График
несимметричен относительно максимума.
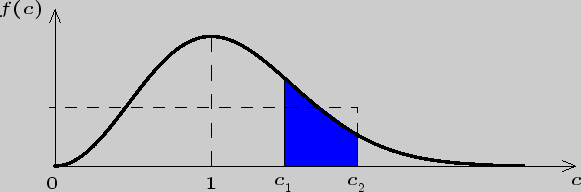
Рис. 4.1
Число молекул ![]() со скоростями в некотором конечном
интервале значений
со скоростями в некотором конечном
интервале значений
![]() (отношение
(отношение
![]() численно равно площади фигуры, заштрихованной на
рис.4.1.) находится интегрированием:
численно равно площади фигуры, заштрихованной на
рис.4.1.) находится интегрированием:
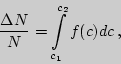
Площадь фигуры, ограниченной кривой и осью абсцисс, равна единице.
Действительно интеграл:
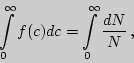
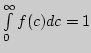 , что
справедливо для всякой функции распределения и называется условием
нормировки.
, что
справедливо для всякой функции распределения и называется условием
нормировки.
В данной работе для изучения особенностей статистических закономерностей
используется нормальное распределение
(Гаусса). Такой вид имеет распределение молекул идеального газа по
составляющим скоростей ![]() ,
, ![]() ,
, ![]() . Оно моделируется на
доске Гальтона -- механической модели, воспроизводящей картину
случайных отклонений от среднего расположения сыпучего вещества на
ней.
. Оно моделируется на
доске Гальтона -- механической модели, воспроизводящей картину
случайных отклонений от среднего расположения сыпучего вещества на
ней.
Нормальное распределение в общем случае имеет вид:
Функция имеет максимум при ![]() . Это значение функции называется
наиболее вероятным.
. Это значение функции называется
наиболее вероятным.
Нормальное распределение имеет место в тех случаях, когда случайная величина зависит от большого числа факторов, которые могут вносить с равной вероятностью положительные и отрицательные отклонения от среднего (наиболее вероятного) значения величины. Примером такого распределения является распределение случайных ошибок измерений.
Рассмотрим влияние параметра ![]() на форму графика. На рисунке
4.2 показан вид таких графиков при различных
на форму графика. На рисунке
4.2 показан вид таких графиков при различных ![]() .
.
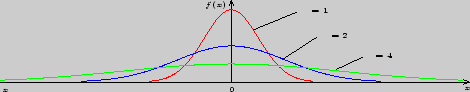
Рис. 4.2
Как видно, чем меньше ![]() , тем больший максимум имеет кривая,
тем круче она идет. Это означает, что вероятность попадания
в некоторый интервал больше для той
случайной величины, распределенной по нормальному закону (с
параметром
, тем больший максимум имеет кривая,
тем круче она идет. Это означает, что вероятность попадания
в некоторый интервал больше для той
случайной величины, распределенной по нормальному закону (с
параметром ![]() ), для которой величина
), для которой величина ![]() меньше. Следовательно,
меньше. Следовательно, ![]() можно
считать характеристикой разброса случайной величины
можно
считать характеристикой разброса случайной величины ![]() .
.
В данной работе нужно на опыте определить
![]() и
получить конкретный вид функции распределения
и
получить конкретный вид функции распределения
![]() .
.
Сходным образом влияет на ход графика функции распределения Максвелла абсолютная температура газа.